5月5日,国际学术期刊eLIFE在线发表了中国科学院上海生命科学研究院生物化学与细胞生物学研究所赵允研究组的最新研究成果——"Set7 mediated Gli3 methylation plays a positive role in the activation of Sonic Hedgehog pathway in mammal"。该项研究揭示了甲基转移酶Set7可以甲基化Sonic Hedgehog(Shh)信号通路的转录因子Gli3,而这种修饰促进了Gli3的癌变(oncogenesis)能力。
Hh信号通路对于动物的早期发育以及成体的稳态维持发挥着重要的作用,它的异常将会导致多种人类严重疾病如肿瘤的发生、发展。一方面,Shh信号通路下游的转录因子包含三个,分别为Gli1, Gli2和Gli3。其中Gli3在有无Shh信号时分别表现全长的激活形式Gli3A和截断的抑制形式Gli3R来发挥作用。因此,对于Gli3的调控对于Shh信号功能尤为重要。另一方面,甲基化修饰对于许多信号通路比如MAPK, BMP, WNT和Hippo等都有十分重要的作用。而其对于Shh信号通路的调控作用还处于未知状态。该研究针对Gli3的功能是否可以被甲基化修饰所调控进行了探索。
在赵允研究员的指导下,博士研究生傅琳首先通过质谱检测发现Gli3的第436位和第595位赖氨酸可以被甲基化修饰。进一步的分析表明,这两个位点有可能是潜在的Set7甲基化位点。随后的体外甲基化实验证实了这两个位点可以被Set7特异性修饰,并发生甲基化。进一步通过制备针对这两点的甲基化抗体,在体内证实了这种修饰的发生。研究表明,甲基化仅仅在Gli3的全长形式Gli3A发生,而Gli3的截短抑制形式Gli3R尽管存在甲基化位点,但不会被Set7说修饰。深入的机制研究表明,Set7所介导的Gli3甲基化修饰能够在Shh存在情况下正向调控Shh信号通路活性。具体来说,436位点的甲基化增强了Gli3的蛋白稳定性而595位点的甲基化提高了Gli3结合Gli1等下游靶基因的能力。同时Shh信号通路的激活可以进一步促进Set7的表达,从而形成一个正反馈调节。动物实验证明,甲基化修饰增强了Gli3的oncogenesis能力,促进了肿瘤的生长和迁移。这一工作由于首次发现Gli分子,特别是Gli3的甲基化,以及Set7这种较为重要的组蛋白甲基化酶对Shh信号通路的非表观遗传调控方式,从而为进一步研究Hh信号通路在癌症,特别是肺癌发生、发展过程的分子机制提供了较为坚实的基础。同时也为人类相关疾病的临床诊治及药物研发提供潜在的靶点。
该研究工作得到生化与细胞所张雷研究员、高大明研究员以及南京医科大学程雁教授的大力协助。该研究的数据收集工作得到生化与细胞所公共技术服务中心细胞分析技术平台、动物实验技术平台、分子生物学技术平台、化学生物学技术平台以及国家蛋白质科学中心·上海(筹)的支持。该研究获得中国科学院及自然科学基金委的基金资助。
文章链接:http://elifesciences.org/content/5/e15690v1
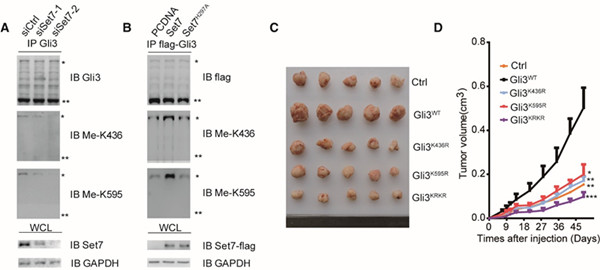
图示:Set7可以在K436和K595位点甲基化修饰全长形式的,并且促进了肿瘤的生长